- تاریخ ثبتنام
- 21/8/19
- ارسالیها
- 1,849
- پسندها
- 75,283
- امتیازها
- 64,873
- مدالها
- 28
- سن
- 23
- نویسنده موضوع
- #1
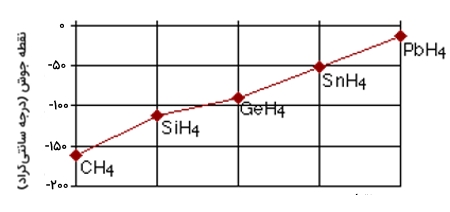
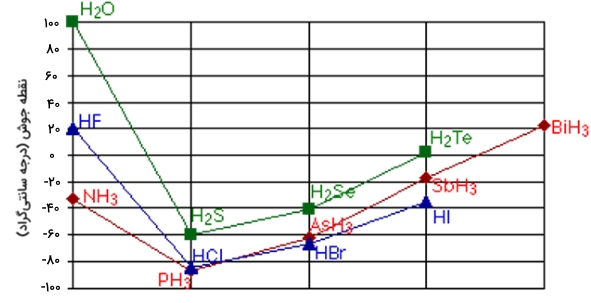
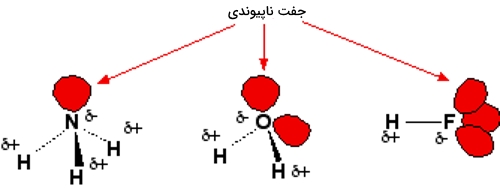
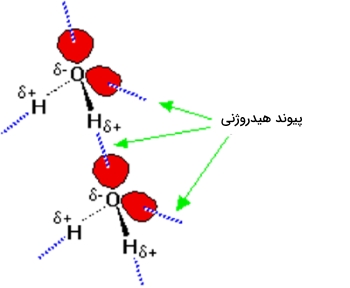
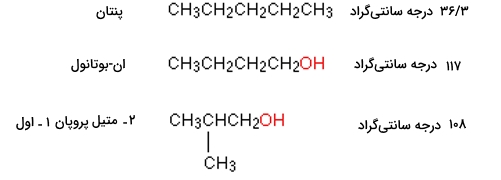
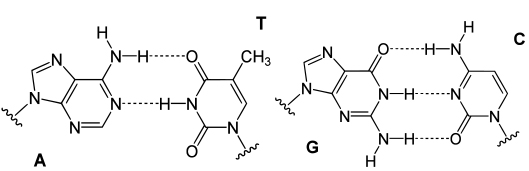
پیوند هیدروژنی نوع ضعیفی از نیروهایی است که موجب ایجاد جاذبه دوقطبی-دوقطبی هستند. این پیوند زمانی تشکیل میشود که یک اتم هیدروژن با اتمی پیوند تشکیل دهد که آن اتم، الکترونگاتیوی بالایی داشته و همزمان در کنار یک اتم الکترونگاتیو دیگری باشد که دارای جفتالکترون ناپیوندی است. این نوع از پیوندها، از نیروهای دوقطبی-دوقطبی معمول و نیروهای پراکندگی، قدرت بیشتری دارند اما ضعیفتر از پیوندهای کووالانسی و یونی هستند.